(11) 97255-6363
unaccam@unaccam.com.br
DIREITO JÁ! Audiência Pública 2022

Há algum tempo, ONGs, associações médicas e pacientes do Sistema Único de Saúde (SUS) têm observado e sofrido com o tempo além do previsto para a disponibilização de medicamentos e tecnologias para o tratamento de câncer de mama e outras neoplasias, que é de até 180 dias após a publicação no Diário Oficial da União (DOU) da decisão da sua inclusão no sistema público de saúde.
A partir disto, a UNACCAM analisou dados públicos, do site do Ministério da Saúde, de Diários Oficiais da União (DOU), solicitados via Lei de Acesso à Informação, entre outros, no intuito de verificar o tempo entre a publicação no DOU até a disponibilização no SUS de todos os medicamentos para câncer de mama aprovados para inclusão no sistema público de saúde desde a criação da Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec), em 2011.
Trastuzumabe: para câncer de mama HER2+
em estágios inicial e localmente avançado
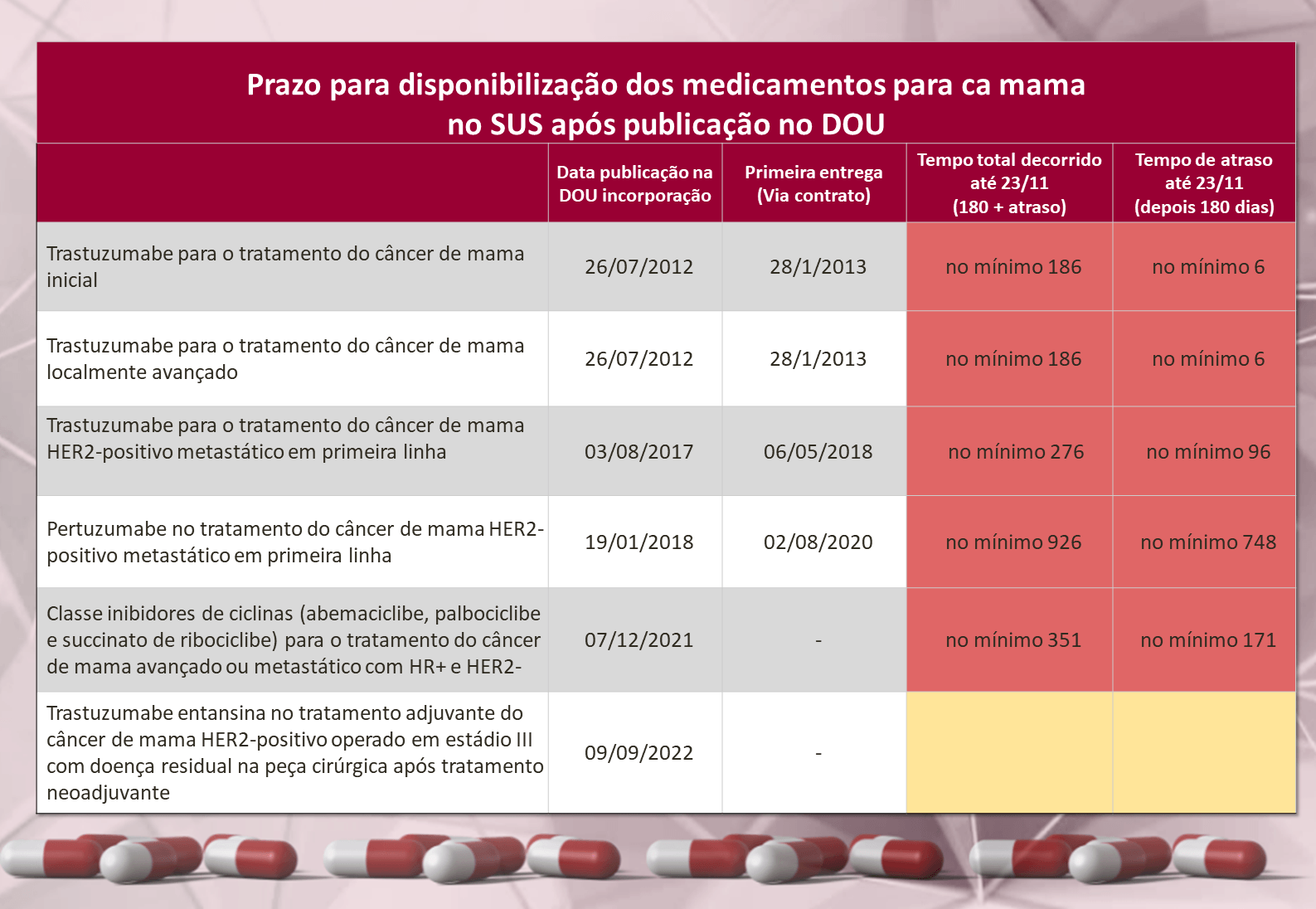
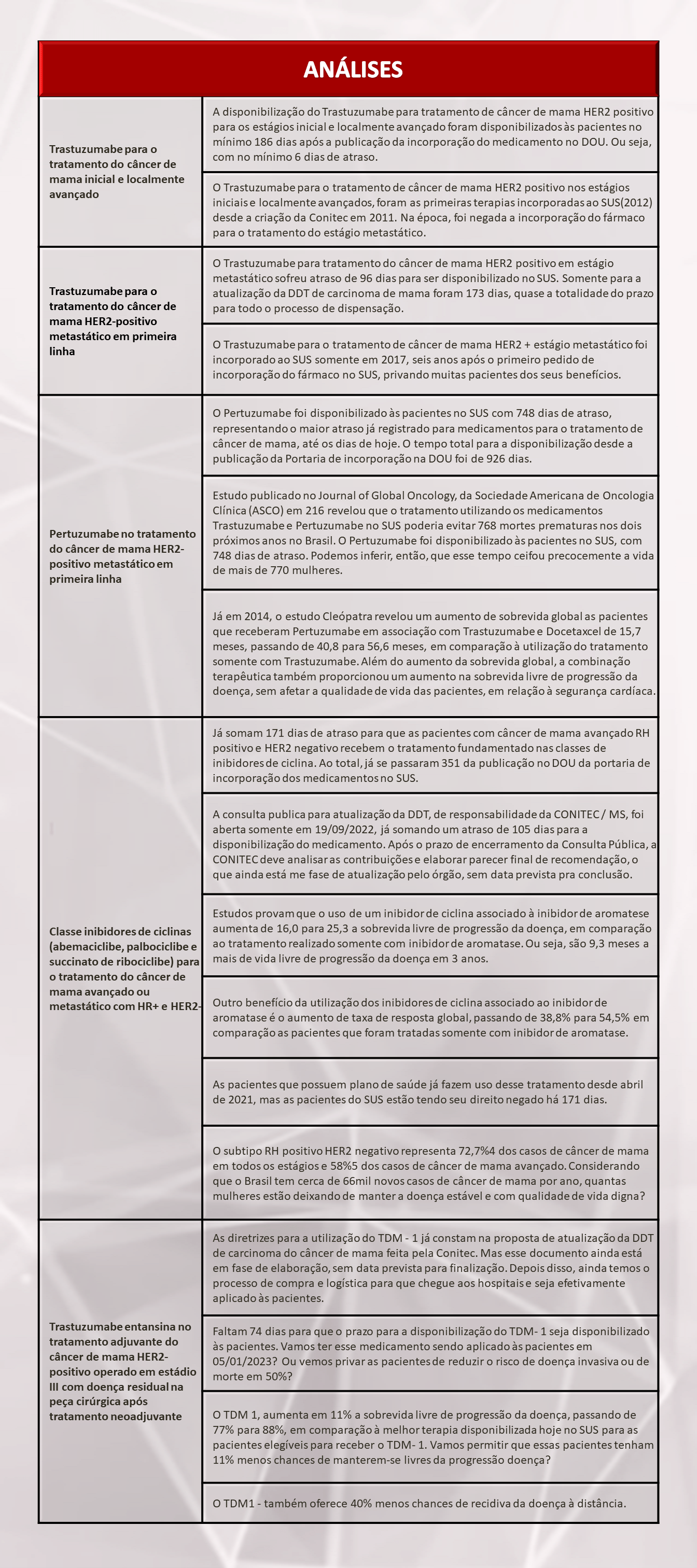
O primeiro medicamento para o câncer de mama incorporado ao SUS após a criação da Conitec foi o Trastuzumabe, para o tratamento do câncer de mama subtipo HER2 positivo em estágios inicial e localmente avançado (I, II e II), em 2012(1). Com o levantamento de dados realizado pela UNACCAM, verificou-se um pequeno atraso de 6 dias para a disponibilização da medicação às pacientes. No total, o processo de dispensação do medicamento levou 186 dias.
Trastuzumabe: para câncer de mama HER2+ em estágio metastático
A primeira solicitação de incorporação do fármaco para o tratamento das pacientes em estágio metastático ocorreu em 2012, juntamente com a solicitação de uso para os estágios inicial e localmente avançado. No entanto, na época o fármaco foi negado às pacientes metastáticas sob alegação de não ser custo-efetivo.
Em 2017 a solicitação para esta indicação de uso foi revista pela CONITEC e, enfim, aprovada. O levantamento de dados realizados pela UNACCAM revelou que o Trastuzumabe para tratamento do câncer de mama subtipo HER2 positivo em estágio metastático ultrapassou em 96 dias o prazo de 180 dias para ser disponibilizado no SUS, ou seja, o tempo total do processo de dispensação foi de 276 dias. Somente para a atualização da DDT de carcinoma de mama foram 173 dias, quase a totalidade do prazo para todo o processo de dispensação.
Pertuzumabe: câncer de mama HER2+ em estágio metastático
O Pertuzumabe teve a solicitação de análise pela CONITEC para inclusão no SUS em 2017. Sua utilização no tratamento das pacientes com câncer de mama subtipo HER2 positivo em estágio metastático é realizada em associação com Trastuzumabe e Docetaxel.
Tendo sua indicação aprovado para inclusão no SUS, foi disponibilizado às pacientes com 748 dias de atraso, ou seja, mais de 2 anos após o prazo de 180 dias previsto em lei, como revelou o estudo realizado pela UNACCAM. Considerando o tempo total para efetiva disponibilização, desde a publicação até a incorporação na DOU, levou 926 dias.
Estudo científico sobre a efetividade do medicamento indicou que pacientes que receberam Pertuzumabe associado ao Trastuzumabe e ao Docetaxel obtiveram um aumento de sobrevida, de 15,7 meses (passando de 40,8 para 56,6 meses) em comparação à utilização do tratamento somente com Trastuzumabe. Além do aumento da sobrevida global, a combinação terapêutica também proporcionou um aumento na sobrevida livre de progressão da doença, sem afetar a qualidade de vida das pacientes, em relação à segurança cardíaca.
Em complemento, o estudo publicado no Journal of Global Oncology, da Sociedade Americana de Oncologia Clínica (ASCO)(2) em 2016 evidenciou que o tratamento utilizando os medicamentos Trastuzumabe e Pertuzumabe em associação com o Docetaxel no SUS poderia evitar 768 mortes prematuras nos dois próximos anos no Brasil. Sendo que o Pertuzumabe foi disponibilizado as pacientes no SUS, com 748 dias de atraso, podemos inferir que esse tempo ceifou precocemente a vida de mais de 750 mulheres.
Classe Inibidores de Ciclinas: RH+ HER2-
para estágios avançado ou metastático
A classe de medicamentos inibidores de ciclina para o tratamento de câncer de mama subtipo RH positivo e HER2 negativo nos estágios avançado e metastático teve sua aprovação para inclusão no SUS publicada no DOU em 07/12/2021. Seu acesso pelas pacientes, de acordo com a lei, deveria ter iniciado até o dia 05/06/2022, no entanto até a data de publicação deste texto (23/11/2022) as pacientes continuam sem receber o tratamento. O atraso já soma 171 dias. Contando o tempo desde a publicação no DOU até a portaria de incorporação dos medicamentos no SUS são 351 dias.
A consulta pública para atualização das Diretrizes Diagnósticas e Terapêuticas (DDT), de responsabilidade da CONITEC / MS, foi aberta somente em 19/09/2022, já somando um atraso de 105 dias para a disponibilização do medicamento no SUS. Após o prazo de encerramento da Consulta Pública, a CONITEC deve analisar as contribuições e elaborar parecer final de recomendação, o que ainda está em fase de atualização pelo órgão, sem data prevista para conclusão.
Estudos provam que estes inibidores, quando associados à aromatase, são capazes de aumentar a sobrevida livre de progressão da doença de 16 para 25, 3 meses em comparação ao tratamento feito apenas com o inibidor. Usando a mesma base de comparação, a resposta global passa de 38,8% para 54,5%.(2)
ATÉ QUANDO AS PACIENTES DO SUS QUE NECESSITAM DESTE TRATAMENTO TERÃO SEU DIREITO NEGADO,
DEIXANDO DE AMPLIAR O SEU TEMPO LIVRE DE PROGRESSÃO DA DOENÇA E MESMO SUA SOBREVIDA GLOBAL?
Trastuzumabe Entansina: adjuvante para HER2 +
operado localmente avançado
Fazer uso do Trastuzumabe Entansina (TDM-1) no tratamento adjuvante do câncer de mama HER2-positivo operado em estádio III com doença residual na peça cirúrgica após tratamento neoadjuvante pode reduzir o risco de doença invasiva ou de morte em 50%.
A APROVAÇÃO PARA SUA INCLUSÃO NO SUS FOI PUBLICADA NO DOU EM 09/09/2022,
TENDO COMO PRAZO PARA A SUA DISPONIBILIZAÇÃO ÀS PACIENTES A DATA DE 05/01/2023.
As diretrizes para a utilização do medicamento já constam na proposta de atualização da DDT de carcinoma do câncer de mama proposta recentemente pela CONITEC, porém o documento, ainda em fase de elaboração, está sem data prevista de finalização, mesmo faltando apenas 74 dias para o prazo de disponibilização do TDM-1 às pacientes. Importante lembrar que ainda há o processo de compra e de logística para que o medicamento chegue aos hospitais e para que seja utilizado em pacientes, o que pode acarretar em mais um descumprimento do prazo de 180 para que as pacientes tenham acesso ao fármaco.
O TDM 1, aumenta em 11% a sobrevida livre de progressão da doença, passando de 77% para 88%, em comparação à melhor terapia disponibilizada hoje no SUS para as pacientes elegíveis para receber o TDM- 1. O tratamento também oferece 40% menos chances de recidiva da doença à distância. Esperamos que esta dispensação ocorra dentro do prazo legal, evitando que as pacientes percam os benefícios citados, que impactam diretamente em sua expectativa e qualidade de vida.
..................................................................
(1) https://oncologiabrasil.com.br/primeira-linha-de-tratamento-do-cancer-de-mama-metastatico-her2/
(2) https://ascopubs.org/doi/pdfdirect/10.1200/JGO.2016.005678
(3) https://mocbrasil.com/blog/mama/novo-inibidor-de-ciclina-aprovado-no-brasil-para-o-tratamento-do-cancer-de-mama-avancado/
-
Dra. Danildes Teixeira
Button"O Objetivo é que nós possamos tratar dessa temática, que tange ao prazo, a identificação do prazo e a incorporação dos medicamentos para o câncer de mama."
-
Dra Danieldes Teixeira Santos
ButtonAdvogada do Corpo Jurídico em Advocacy da UNACCAM
-
Dr. Paulo Benevento
Button"A integralidade da assistência terapêutica, hoje, está vinculada a um processo de avaliação de tecnologias(...) Essa avaliação leva tempo (...) Tempo, esse, que deveria estar na lei."
-
Dr. Paulo Benevento
ButtonAdvogado responsável pelo corpo de Advocacy da UNACCAM
-
Deputada Flavia Moraes
ButtonDeputada responsável pela petição da Audiência Pública dentro da Câmara dos Deputados em Brasília
-
Dep. Flavia Moraes
Button"O interesse maior que deve ser o interesse de todos nós, que é a vida! Principalmente daqueles pacientes que venham a ter um câncer em estágio avançado."
OBJETIVO - Identificação do prazo entre a publicação da incorporação de medicamentos para câncer de mama no DOU e sua disponibilização às pacientes.
ANÁLISE DE DADOS
Relatório de Avaliação da Controladoria-Geral da União (CGU) publicado em 2021(3) analisou, entre outras questões, o prazo entre a publicação da incorporação de 25 tecnologias, entre os anos de 2017 e 2019, e sua efetiva disponibilização no SUS a fim de identificar, entre outras demandas, se as etapas prévias à tal dispensação ocorriam de fato no prazo de 180 dias. Vale destacar que dentre as 25 tecnologias avaliadas pela CGU constam tratamentos para diferentes enfermidades, não restringindo-se somente à oncologia, tampouco ao câncer de mama.
O resultado obtido com o estudo é estarrecedor: o prazo médio decorrido entre a data da incorporação e a efetiva dispensação foi de 624 dias. É relevante destacar que “para nenhum dos 25 casos selecionados houve o cumprimento do prazo de 180 dias para oferta do medicamento no SUS.”(4)
Destaca-se também a intempestividade na realização de diversas etapas necessárias ao alcance dos seus objetivos: O tempo médio para finalização dos processos de ATS conduzidos nos 3 exercícios avaliados excedeu o prazo ordinário de 180 dias previsto na legislação e as etapas subsequentes à publicação da Portaria de incorporação têm gerado atrasos na efetiva disponibilização do medicamento aos usuários do SUS, que atingiram, na média, 624 dias, o equivalente a 3,5 vezes o prazo legalmente previsto.
Ao aprofundar o estudo, selecionando 9 tecnologias com atraso igual ou superior a dois anos para disponibilização no SUS, dentre as 25 analisadas inicialmente, foi identificado um período médio de 828 dias para que os pacientes tivessem acesso a estes tratamentos.
Os motivos dos atrasos na dispensação dos medicamentos devem-se, segundo o relatório da CGU, ao longo período levado pela Comissão Inter Partite (CIT) realizar a pactuação para o financiamento dos medicamentos, que revelou-se ser em média de 300 dias. Agrega-se a esse período outras etapas do processo como a aquisição das tecnologias pelo Departamento de Logística do Ministério da Saúde (DLOG), que revelou-se ser em média de 265 dias e da inclusão do seu código no SIGTAP, “também consomem parcela significativa do prazo”.
Diante deste cenário e da percepção já frequente dos atrasos para a dispensação dos medicamentos para câncer de mama, a UNACCAM realizou o levantamento de dados que expõe o prazo entre a incorporação dos medicamentos no SUS e a sua efetiva disponibilização às pacientes. Por outro lado, a transparência dos atos relacionados à avaliação de tecnologias no SUS foi destacada pelo CGU. O site da Conitec disponibiliza diversas informações a qualquer cidadão.
Com a pesquisa, foram emitidas recomendações à Secretaria de Ciência, Tecnologia, Inovação e Insumos Estratégicos em Saúde e à Secretaria-Executiva do Ministério da Saúde na busca pela qualificação do processo de incorporação de tecnologias e pela obliteração de riscos que possam impactar-lo negativamente.
CENÁRIO GERAL SOBRE O DESCUMPRIMENTO DO PRAZO DE 180 DIAS PARA OFERTA DE MEDICAMENTOS AOS PACIENTES DO SUS APÓS SUA INCORPORAÇÃO.
Informações de qualidade para Multiplicar sobre Saúde da Mama
Copyright UNACCAM 2020| Todos os Direitos Reservados |